Tiedot sijoituksesta
- Tyyppi:
- Osakeanti
- Sijoitettu:
- 2 000 367,00 €
- Jaettava omistusosuus:
- 3,34 – 14,75 %
- Osakkeen hinta :
-
3,00 €
minimisijoitus 400 osaketta
- Osakkeiden nykyinen lukumäärä:
- 3 853 523
- Osakekanta täyden diluution jälkeen:
- 3 973 523
- Valuaatio (pre-money):
- 11 560 569,00 €
Tarinamme
IQ-Tip®️ - Teknologiaa lääkäreiltä lääkäreille
Kolme lääketieteen ja lääketieteellisen tekniikan huippuosaajaa pohti sokkona tehtävän lannepiston ongelmaa Tampereella jo yli 10 vuotta sitten ja päätti lähteä kehittämään älyneulaa, joka ratkaisisi tämän ongelman. Tuloksena on syntynyt Injeqin selkäydinnesteen tunnistava IQ-Tip®️ älyneula.
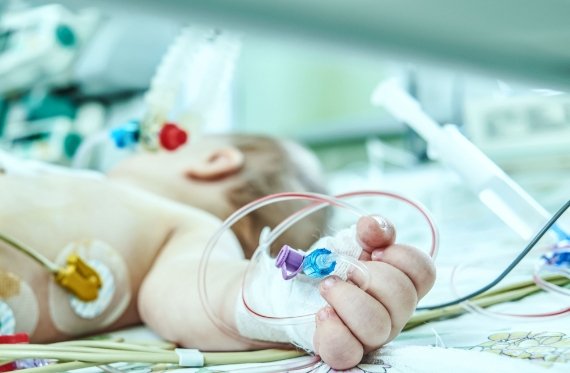
Injeq Oy perustettiin, kun jo aiemmin tunnistettu lääketieteellinen tarve yhdistyi teknologiaosaajien näkemykseen sen mahdollisesta ratkaisusta. Riitan, Katjan ja Jarin visio älyneulasta on edennyt valmiiksi tuotteeksi, joka voidaan pian saada kliiniseen käyttöön. Tänä päivänä neulan CE-sertifiointi on lähes valmis ja vuodenvaihteen jälkeen tuote saataneen markkinoille. Saadessaan myyntiluvan alkuvuodesta 2021 tullaan IQ-Tip® älyneulaa ensin käyttämään vaativissa lannepistoissa eli lumbaalipunktioissa syöpäosastoilla lasten leukemian hoitoon liittyvissä punktioissa sekä vastasyntyneiden teho-osastoilla. IQ-Tip® älyneulalla on kliinisissä kokeissa todettu hyvä ensimmäisen piston onnistumisprosentti kirjallisuuteen verrattuna ja sen odotetaan nostavan onnistumismahdollisuuksia myös kaikkein pienimmille potilaille tehtävissä haastavissa lumbaalipunktioissa. Leukemialapset ja vastasyntyneet vauvat ovat vain esimerkkejä potilaista, jotka hyötyvät Injeqin älyneulan tunnistustekniikasta.
Injeq IQ-Tip®️ älyneula - Tavoitteena turvallisuus vaativissa pistoissa
Akuutti lymfaattinen leukemia eli ALL on lasten yleisin syöpäsairaus. Heti taudin alussa lapsen selkäydinnesteestä otetaan näyte lumbaalipunktiolla eli otetaan neulalla näyte selkäydinkanavasta lannerangan korkeudelta. Näytteestä voidaan arvioida syöpäsolujen levinneisyys keskushermoston alueelle. Jatkossa lumbaalipunktioita käytetään taudin seurantaan ja syöpälääkkeiden annostelemiseen aivoselkäydinnesteen joukkoon. ALL-lapselle tehtävä punktio on kriittinen - etenkin jos tauti ei ole vielä levinnyt keskushermostoon. Mikäli punktio ei onnistu optimaalisesti on mahdollista, että syöpäsoluja pääsee leviämään veren mukana selkäydinkanavaan. Tämä aiheuttaa riskin taudin leviämiselle keskushermoston ja aivojen alueelle. Leukemian ennusteen kannalta on tärkeää minimoida tämä mahdollisuus. Siksi turvallinen lumbaalipunktio on erittäin tärkeä ja toimenpiteen onnistuminen heti ensiyrittämällä on maksimoitava käyttämällä Injeqin älyneulaa. Syksyllä 2020 päättyneen Injeqin IQ-LP-03 kliinisen tutkimuksen mukaan IQ-Tip® älyneulaa käytettäessä lannepisto onnistui heti ensimmäisellä kerralla huomattavasti useammin kuin kirjallisuuden mukaan vastaavassa potilasryhmässä pistettäessä perinteisellä neulalla.
Aikaisemmin ALL-lapsia hoidettiin Suomessa yhteispohjoismaisen NOPHO – ALL 2008 -hoitoprotokollan mukaan. Tällä hoito-ohjelmalla jopa yli 90% ALL-lapsipotilaista paranee, mutta kuitenkin lapsia kuolee edelleen tähän tautiin ja rankkojen hoitojen seurauksiin. Tunnistettiin tarve optimoida protokollaa; suuremman riskiluokan potilaat tarvitsisivat kovempaa ja matalamman riskin potilaat kevyempää hoitoa. Syntyi 13 Euroopan maan yhteinen ALLTogether tutkimus, johon Suomi liittyi muiden pohjoismaiden kanssa vuonna 2019. Tutkimuksen hoitoprotokollan tavoitteena on edesauttaa taudista selviytymistä ja selviytymisen laatua.
Vaikka suurin osa selviää, edelleen on ALL-lapsipotilaita, jotka kuolevat taudin uusiutuessa. Tämän ajatellaan johtuvan riittämättömästä hoidosta, ns. ”under-treatmentista”. Toisaalta huomattava osa nuorista potilaista kuuluu ns. ”over-treated” ryhmään, minkä seurauksena hoidosta johtuvien kuolemien, pitkäaikaisten sivuvaikutusten ja myöhemmin kehittyvien sekundääristen syöpien riski on kohonnut. ALL-taudista johtuva kuolleisuus on lähes samalla tasolla kuin taudin hoidosta johtuva kuolleisuus. Hoidosta johtuvia riskejä kuten verenvuotoon johtavia lumbaalipunktiota voidaan vähentää optimoimalla piston suorittaminen IQ-Tip® älyneulaa käyttämällä. Ajallisesti tämä meistä riippumaton tutkimus tarjoaa optimaalisen väylän jakelijoillemme lähestyä ALL-lapsia hoitavia lääkäreitä IQ-Tip® älyneulan kanssa. Yhteinen tahtotila ALLTogether tutkimuksella ja Injeqillä on pienten potilaiden laadukas hoito tavoitteena pelastaa myös se “viimeinen” 10% ALL:aan sairastuneista lapsista elämälle.
Injeq IQ-Tip® älyneulaa on tutkittu myös aivan pienten vastasyntyneiden vauvojen lumbaalipunktioissa vuonna 2018 päättyneessä tutkimuksessa. Vastasyntyneet vauvat ovat ensimmäisen elinkuukautensa aikana alttiita aivokalvontulehdukselle. Tila on vakava ja diagnosoimattomana saattaa johtaa nopeasti kuolemaan. Diagnostinen lumbaalipunktio on kuitenkin erityisen haastava, koska toimenpide tehdään yleensä ilman anestesiaa. Injeq on mukana helpottamassa myös kaikkein pienimpien alkutaivalta. Älyneulan uskotaan vähentävän ylimääräisten punktioiden tarvetta, jouduttavan diagnoosin saamista ja siten vähentävän myös sairaalapäiviä ja kustannuksia.
Tapausesimerkkinä kliinisestä tutkimuksestamme voidaan mainita kahden päivän ikäinen vauva, jolta näytteenotto selkäydinnesteestä ei onnistunut normaalilla neulalla edes neljällä yrityksellä. Älyneulalla toimenpide onnistui heti, ensi yrittämällä. Älyneulaa on onnistuneesti käytetty kliinisissä tutkimuksessamme myös 1,4-kiloisella keskosvauvalle tehdyssä pistossa.
Älyneulan toiminta on ainutlaatuinen
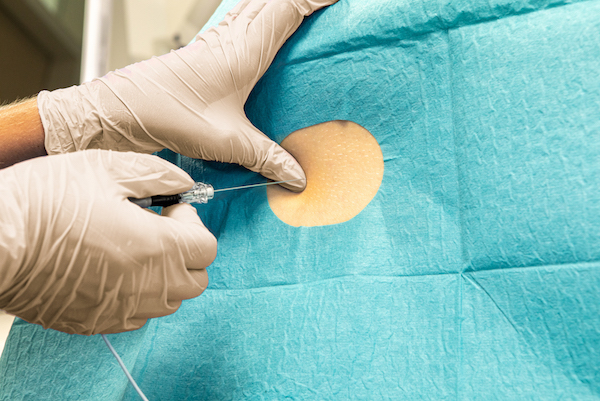
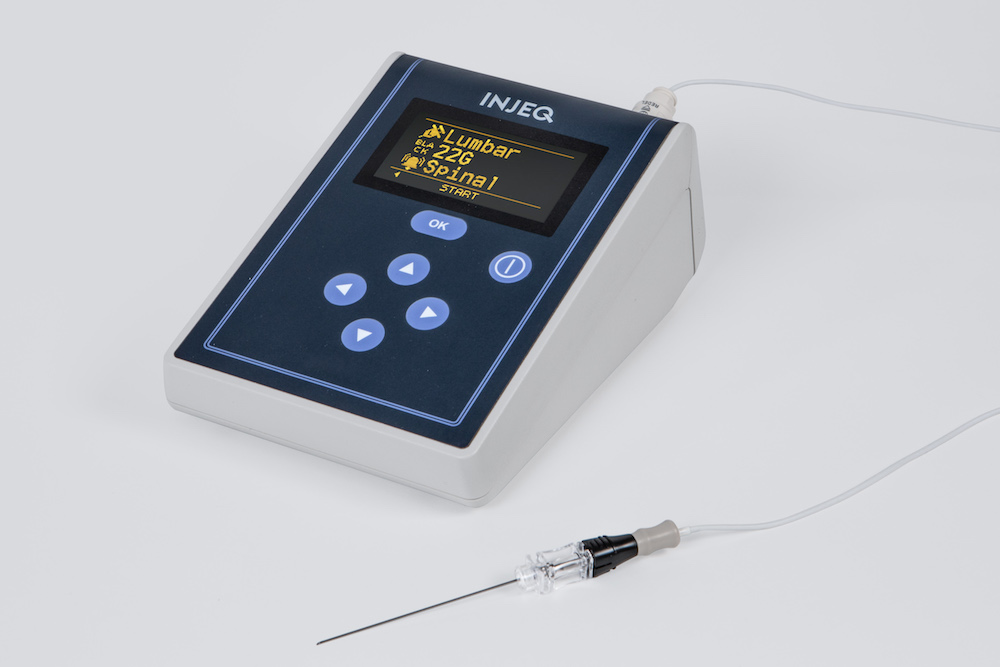
Injeq IQ-Tip®️ älyneulan toimintatapa on ainutlaatuinen: neulan runkoa ja sen sisällä olevaa mandriinia (styletti) käytetään piston aikana mittauselektrodeina, joiden kautta mitataan neulan kärkeä koskettavan kudoksen bioimpedanssi. Injeq IQ-Tip®️ analysaattori tekee tämän 200 kertaa sekunnissa, viidellätoista eri taajuudella. Näin pystytään päättelemään reaaliaikaisesti milloin neulan kärki saavuttaa kohteensa. Lumbaalipunktion aikana älyneula ilmoittaa analysaattorin näytön lisäksi myös äänimerkillä heti neulan kärjen koskettaessa selkäydinnestettä, eli kun neula on perillä kohteessaan selkäydinkanavassa.
Selkäydinnesteen tunnistusta ja laitteiston turvallisuutta olemme tutkineet kolmessa kliinisessä tutkimuksessa, joissa on tehty yhteensä 261 älyneula-avusteista lumbaalipunktiota. Lisätietoja älyneulan toiminnasta ja aiemmin julkaistuista kliinisistä tutkimuksistamme on löydettävissä yhtiön kotisivuilta julkaisut-osiosta.
Käyttökohteiden moninaisuus muodostaa laajan markkinapotentiaalin
IQ-Tip®️ älyneulalla tulee olemaan useita sovelluksia. Lannepistojen osalta vaativimpia toimenpiteitä ovat vastasyntyneiden ja ALL-lasten punktiot. Tässä kohderyhmässä älyneulan hyödyt ja tarve ovat niin ilmeisiä, että mainitut punktiot ovat älyneulan ensimmäisiä kaupallisia sovelluksia. Muita mahdollisia sovelluksia - vaatien osin uusia kliinisiä kokeita ja tuoteversioita - ovat esimerkiksi syöpälääkkeiden injektiot, sisäelinten syöpänäytteenotot, selkäydinnestetilan varjoainetutkimus, lumbaalipunktiot Alzheimerin taudin diagnosoinnissa, nivelpistot ja verisuonipistot. Mainitut kliiniset sovellukset tarjoavat laajalti tulevaisuuden kasvumahdollisuuksia. Pitkällä tähtäimellä voidaan pohtia myös ensihoidon ja sotilaslääketieteen kenttäolosuhteiden tarjoamia erityisiä sovellusalueita, joissa esimerkiksi pikainen apu saadaan oikein perille haastavissakin olosuhteissa. Jokainen sovelluskohde muodostaa jo yksinään huomattavan markkinan ja markkinapotentiaali on siten kokonaisuudessaan laaja.
Injeq älyneulaa tavoitellaan osaksi normaalia hoitokäytäntöä
Injeq IQ-Tip®️ älyneulaa vastaavaa tuotetta ei ole markkinoilla, eikä yhtiö ole tietoinen potentiaalisista kilpailijoista, jotka olisivat lähellä markkinoille tuloa. Vastaavaa injektointia helpottavaa toiminnallisuutta on kehitetty eri tutkimusryhmissä esimerkiksi paineentunnistukseen tai valon heijastumiseen perustuvilla tekniikoilla. Näillä tekniikoilla ja käytettävyydellä on kuitenkin puutteensa ja niiden mahdollisesta markkinoille tulosta ei ole tarkempaa tietoa. Yhtiöllä on siten erinomainen tilaisuus saavuttaa asema uutena standardina hoitotoimenpiteissä, joissa tehdään vaativia pistoja. Kliinisissä potilastutkimuksissa Injeq IQ-Tip®️ älyneula on todettu toimivaksi ja turvalliseksi. Tuote on valmiina markkinoille tuotavaksi heti, kun IQ-Tip®️ älyneulan kliininen arviointi on hyväksytty ilmoitetun laitoksen toimesta ja tuotteen rekisteröinti on onnistuneesti suoritettu tiukentuneiden regulaatiovaatimusten (MDR, Medical Device Regulation) mukaisesti. Yhtiö arvioi tämän tapahtuvan vuoden 2021 alussa.
Miksi sijoittaa Injeqiin?
Yhtiöllä on kliinisten potilastutkimusten jälkeen käsissään ainutlaatuinen tuote - IQ-Tip®️ älyneula – valmiina kaupallistettavaksi kasvaville terveydenhuollon markkinoille mahdollistaen potilaille tehtävien haastavien lannepistojen onnistumisen entistä paremmin ja turvallisemmin.
- Yhtiö odottaa laatujärjestelmän sertifioinnin ja tuotteiden CE-sertifioinnin valmistuvan tammi-helmikuun 2021 aikana mahdollistaen myynnin käynnistämisen Euroopassa.
- Kliiniset potilastutkimukset on saatu valmiiksi hyvin tuloksin. Yhtiö on kaupallistamassa ensimmäiset tuotteensa uusimman MD-asetuksen (MDR, Medical Device Regulation) korkean vaatimustason mukaisesti.
- Tuotteen viranomaishyväksyntä- ja ns. myyntilupaprosessi auditointeineen on jo loppuvaiheessa ilmoitetun laitoksen toimesta.
- Yhtiöllä on osaava ja kokenut henkilöstö, joka sidosryhmineen kykenee kaupallistamaan vaativat lääketieteellisen tekniikan tuotteet alkaen älyneulasta yhtiön ensimmäisenä tuotteena.
- Älyneula pyrkii tekemään haasteelliset lannepistot ja myöhemmin myös muut vaativat pistot entistä turvallisemmiksi potilaille.
- Yhtiö pyrkii osaltaan auttamaan leukemiaa sairastavien lasten hoidossa ja vähentämään traumaattisten lannepistojen haittavaikutuksia yhä useammalla potilaalla.
- Uudet sovellusalueet ja yhtiön tutkimuksissa kerätyt asiakastarpeet ja käyttäjäpalautteet tarjoavat monipuolisia tuote- ja kasvumahdollisuuksia yhtiön toimiala- ja prosessi- ja kaupallisen osaamisen hyödyntämiseen.
- Yhtiö on turvannut immateriaalioikeuksiaan suojaamalla teknologiaansa patenteilla.
- Sijoituskohteena yhdistämme taloudellisen tuloksen tavoittelemisen eettisiin tavoitteisiin. Yhtiönä Injeq pyrkii ensisijaisesti kehittämään uusia menetelmiä ja hoitokäytäntöjä potilaan parhaaksi - mikä on avain menestyksekkääseen ja kestävään liiketoimintaan vaativalla lääketieteellisen tekniikan sektorilla.
Mitä olemme saavuttaneet edellisen rahoituskierroksen jälkeen
Kesällä 2019 toteutetun edellisen Invesdorin kanssa toteutetun rahoituskierroksen jälkeen on tapahtunut paljon. Tärkeintä on, että MD-asetuksen mukainen tuotehyväksyntä- ja myyntilupaprosessi IQ-Tip®️ älyneulalle on käynnissä ilmoitetun laitoksen TÜV SÜD:in kanssa.
Vuonna 2019 löysimme uudet sopivat toimitilat, joissa on yhtiölle sopivat tuotanto- ja puhdastilat. Tuotehyväksyntään kuuluvien toimenpiteiden ohella olemme myös rekrytoineet uusia loistavia ammattilaisia, rakentaneet tulevaa jakelu- ja myyntiverkostoamme ja ylläpitäneet patenttiportfoliotamme.
Vuonna 2020 yhtiölle on myönnetty kolme patenttia, kaksi USA:ssa sekä näistä biopsianeulaan liittyvä patentti lisäksi myös Euroopassa. Toinen USA:ssa myönnetyistä patenteista laajentaa kaupallistamisvaiheessa olevassa ensimmäisessä tuotteessamme sovellettavan keksinnön suojausta Euroopan ulkopuolelle.
Lääkinnällisille laitteille sovellettava uusi MD-asetus on merkittävästi vaikeuttanut laitevalmistajien tuotteiden hyväksyntämenettelyyn vaadittujen ilmoitettujen laitosten (Notified Body) saatavuutta erityisesti alan uusille toimijoille. Vahvistettuja uuden MD-asetuksen mukaisia ilmoitettuja laitoksia oli koko Euroopassa keväällä 2020 rekisteröintiprosessimme alkaessa vain hieman yli kymmenen aiemman noin viidenkymmenen asemesta. Tässä markkinatilanteessa lääkinnällisten laitteiden CE-sertifointia jatkavat laitokset valitsevat asiakkaansa tarkkaan. Voimme olla tyytyväisiä, että olemme päässeet sopimukseen asiakkuudesta arvostetun TUV SUD:n kanssa.
Samalla olemme keskittyneet saattamaan prosessimme ja laatujärjestelmämme valmiiksi ja vaatimusten mukaisiksi myyntiluvan myöntämistä varten. Tämä on kaiken kaikkiaan aikaa vievä prosessi - erityisesti kolmanteen vaativuusluokkaan kuuluvan älyneulamme osalta. Täyttääksemme kaikki tuotteelle ja tuotannolle asetetut vaatimukset sen koko elinkaaren aikaiset riskit minimoiden, meidän on täytynyt suorittaa laaja määrä tuotehyväksyntätestejä ja mm. prosessien validointeja. Jokaisen tuotantoprosessin vaiheen kelpoisuus tuotantoon on todistettu moniosaisen validointimenettelyn avulla. Validointien tarkastus ilmoitetun laitoksen toimesta on osa tuotehyväksyntäprosessia.
Kuluneen vuoden keskeisin tavoite laatujärjestelmän sertifioinnin ohella on ollut kliinisen potilastutkimuksen ja sen pohjalta tehtävän CE-hyväksyntäprosessin loppuunsaattaminen MD-asetuksen mukaisesti. Marraskuussa 2019 käynnistynyt kliininen potilastutkimuksemme eteni poikkeusoloista huolimatta hyvin loppuun saakka. Suunnitellun potilas- ja toimenpidemäärän täytyttyä ja kuukauden seurantajakson päätyttyä viimeisimpien potilaiden osalta saimme tutkimuksen päätökseen syyskuussa 2020. 50 ALL-lapsipotilasta ja 152 toimenpidettä käsittävän tutkimuksen tulokset on sen jälkeen analysoitu yhdessä tutkijoiden kanssa. Piston onnistuminen ensimmäisellä yrityksellä oli merkitsevästi parempi kuin alun perin asettamamme kirjallisuuteen perustuva tutkimuksen hyväksymisraja. Toinen merkittävä hyöty liittyi selkäydinnestenäytteen laatuun, jossa täysin verettömien näytteiden osuus oli merkitsevästi suurempi kuin vertailuaineistossa. Myös lannepiston yleisintä ei-toivottua jälkiseuraamusta, eli punktion jälkeistä päänsärkyä, esiintyi tutkimusaineistossamme vähemmän kuin arvostetussa The Lancet – lehdessä vuonna 2018 julkaistussa meta-analyysissä ja katsausartikkelissa raportoitiin. Yksityiskohtaiset tulokset tullaan julkaisemaan kansainvälisessä alan ammattilaisille suunnatussa tieteellisessä julkaisussa.
Käyttämämme ilmoitetun laitoksen (Notified Body) TÜV SÜDin auditointi on käynnissä osana sertifiointiprosessia myyntiluvan saamiseksi tuotteellemme. Laatujärjestelmämme ensiauditointi on syksyn ajan poikkeusoloista huolimatta edennyt sujuvasti. TÜV SÜDin asiantuntijat vierailivat äskettäin auditoimassa prosessimme ja puhdastilamme todeten ne asianmukaisiksi. Auditoinnissa tähän saakka ilmenneisiin havaintoihin olemme jo vastanneet. Luokan 3 tuotteen, eli neulan, teknisen dokumentaation tarkastus ja arviointi on parhaillaan käynnissä viimeisenä auditoinnin osiona. Rekisteröintiprosessi on siten osaltamme aivan loppusuoralla. Tarvittavat tärkeimmät kehitystoimenpiteet tulemme tekemään jo marras-joulukuun aikana ja luvan tuotteiden myyntiin arvioimme saavamme 2021 alussa riippuen ilmoitetun laitoksen ja EU:n prosesseista, jotka tulevat viemään hieman aikaa vielä auditoinnin jälkeen.

Liiketoiminta- & markkinatilanteemme
Tuote ja kysyntä
Yhtiön ensimmäinen tuote on IQ-Tip®️ spinaalineula, jolla voidaan sekä ottaa näyte selkäydinnesteestä (cerebrospinal fluid, CSF) että annostella selkäydinnesteeseen lääkeaineita esimerkiksi leukemiahoidon yhteydessä. Nämä lumbaalipunktiot ovat erityisen vaativia pienillä lapsilla, ja erityisesti pohjoismaiset yliopistolliset lastensairaalat ovat osoittaneet suurta kiinnostusta saada tuote käyttöönsä. Lasten yleisimmässä syöpäsairaudessa, eli ALL-tyypin leukemiassa, lumbaalipunktio tehdään yhdelle potilaalle tyypillisesti noin 20 kertaa. Toimenpiteeseen liittyvät riskit voivat johtaa vaurioihin, lisätä kipua ja kärsimystä ja hankaloittaa hoitoa. Laajan kanadalaisen tutkimuksen mukaan traumaattiseen lumbaalipunktioon liittyvä verenvuoto selkäydintilaan johtaa pienempään selviytymistodennäköisyyteen (Shaikh ym. 2014).
Syöpähoitojen ohella toinen tyypillinen syy lumbaalipunktioon on aivokalvontulehdusepäily, jonka diagnosoinnissa laadukas selkäydinnestenäyte on tarpeen. Hoitamaton tai huonon näytteen vuoksi diagnosoimatta jäänyt aivokalvontulehdus on aina hengenvaarallinen. Vastasyntyneiden kohdalla tällaisen näytteen saamiseen liittyy ongelmia, joita Injeq IQ-Tip®️ älyneulan käytön odotetaan ratkaisevan. Tutkimusten mukaan n. 50 % vastasyntyneiden pistoista epäonnistuu tai aiheuttaa kudosvaurioita (Olowoyeye, 2019). Epäonnistuneet pistot, huonolaatuiset näytteet ja niistä seuranneet viivästykset hoidossa sekä potilaalle aiheutuvat mahdolliset uusintakäynnit aiheuttavat kivun ja kärsimyksen lisäksi kuluja lapsen tehohoidon venyessä tarpeettomasti.
Tuotteemme odotetaan tarjoavan etuja myös aikuisille tehtävissä toimenpiteissä. Tavoite on, että älyneulan saatua aseman lasten lumbaalipunktioissa, menetelmä otetaan käyttöön ensin aikuisille tehtävissä haastavissa lumbaalipunktioissa, joista se voi edelleen levitä jokapäiväiseen käyttöön kaikille potilasryhmille.
Liiketoimintamalli
Markkinapotentiaali eurooppalaisissa lastensairaaloissa arvioidaan olevan yli 50 M€ vuodessa pohjautuen potilas- ja toimenpidemääriin, sairaaloiden lukumäärään ja arvioituihin myyntihintoihin. Suurin tarve tuotteille on lasten leukemiahoidoissa sekä vastasyntyneiden diagnostiikassa ja tehohoidossa. Nämä erikoisalat kattavat noin 60% lasten toimenpidemääristä. Myyntistrategiana katamme kunkin lastensairaalan vaativien lumbaalipunktioiden kokonaistarpeen kohtuullisen siirtymäajan puitteissa, jolloin toimintatavat pysyvät mahdollisimman yhtenäisinä.
Injeqin älyneulan potentiaalisen kokonaismarkkinan (potential available market, PAM) voidaan ajatella kattavan maailmanlaajuisen spinaalineulojen kulutuksen kaikissa mahdollisissa pistoissa. Tämä olisi luonnollisesti arvoltaan useita miljardeja euroja. Kokonaismarkkina (total available market, TAM) on merkittävästi pienempi. Kun tavoittelemme globaalia markkinaa vain sovelluksissa, joissa IQ-Tip®️ teknologia tarjoaa merkittävän lisäedun olemassa olevaan toimenpiteeseen nykytuotteisiin verrattuna, pienenee markkina edelleen, jolloin palveltavan markkinan (serviceable available market, SAM) arvioidaan olevan miljardin euron luokkaa, riippuen hintaeroosiosta tulevaisuudessa.
Sekä myyntitapa että hinnoittelumalli tulevat vaihtelemaan kohdemarkkinan ja osin jakelijakumppanin mukaan. Tuotekokonaisuuteen kuuluvat kudosanalysaattori, kertakäyttöinen neula ja näiden välinen kaapeli. Analysaattoreiden myynti kertaluonteisena kauppana tuo nopeammin tulovirtaa ja myynti loppuasiakkaalle käynnistää älyneulojen myynnin kertakäyttötuotteina. Kohdemarkkinasta ja jakelijoidemme käyttämistä rahoitusmalleista riippuen analysaattorit tullaan kuitenkin usein sijoittamaan asiakkaille leasing-rahoituksella tai vuokraamalla, mikä madaltaa hankintakynnystä. Osa voidaan luonnollisesti sijoittaa suoraan, jolloin hankinta kohdistuu pelkästään kulutustavaroina myytäviin tuotteisiin. Eri kohdemarkkinoille sopivia liiketoiminta- ja hinnoittelumalleja tullaan tarkastelemaan jakelijoidemme kanssa lisäksi siten, että hinnoittelu erityisesti mielipidejohtajille sekä aikaisen vaiheen käyttäjille tukee nopeampaa markkinapenetraatiota. Pyrimme käynnistämään paikallisia tutkimuksia ja niiden myötä julkaisuja kohdemarkkinoilla osoittaen tuotteen toimivuuden ja käytettävyyden paikallisellakin tasolla.
Myynti, valmistus ja jakelu
Tuotteidemme myynti ja markkinointi Euroopassa edellyttää MD-asetuksen mukaista tuotehyväksyntää ja sertifiointia (CE-merkintä) ilmoitetun laitoksen ja älyneulamme osalta myös EU:n toimesta. Yhtiö arvioi saavansa tarvittavat rekisteröintivaiheen tehtävät omalta osaltaan päätökseen vuoden 2020 lopussa. Ilmoitetun laitoksen ja EU:n prosessien myötä lopullisen rekisteröinnin arvioimme toteutuvan 2021 alkuvuodesta.
Ensimmäisenä myyntikohteena ovat Euroopan lastensairaalat, joissa tuotteitamme tullaan käyttämään lumbaalipunktioiden onnistumisen ja turvallisuuden parantamiseksi. Lastensairaaloita toimii sekä yliopistosairaaloiden että synnytyssairaaloiden yhteydessä ja myös erillisinä yksiköinä. Myyntiponnistelut keskitetään alkuvaiheessa erityisesti johtaviin yliopistosairaaloihin, jotka toimivat samalla referensseinä ja edistävät Injeqin laitteiden käyttöä osana uutta eurooppalaista ALLTogether hoitokäytäntöä erityisesti ALL-tyypin leukemiassa ja muissa vaativissa lumbaalipunktioissa.
Injeq omistaa keskeiset oikeudet tuotteisiinsa ja toimii niiden valmistajana vastaten niiden turvallisuudesta. Neula ja kaapeli valmistetaan yhtiön tuotantotiloissa Tampereella komponenteista, joita hankitaan useilta eri valmistajilta. Yhtiö on muuttanut kesällä 2019 uusiin toimitiloihin Tampereen yliopistollisen sairaalan alueelle. Asianmukaiset toimitilat mahdollistavat tuotannon kasvattamisen myynnin kasvaessa. Tuotteiden sterilointi tapahtuu eurooppalaisen yhteistyökumppanin toimesta. Analysaattorit valmistaa kotimainen sopimusvalmistaja.
Myynti toteutetaan paikallisten jakelijoiden kanssa, ensisijaisesti sellaisten alueellisten toimijoiden kanssa, jotka ovat jo vakiintuneita paikallisia toimijoita lastensairaaloiden kanssa. Injeq on identifioinut noin 450 mahdollista toimijaa/jakelijaa maailmalla, joista useat eurooppalaiset jakelijat on edelleen valittu yksityiskohtaisempiin neuvotteluihin. Jälleenmyynti on alustavasti sovittu viiteen Euroopan maahan ja keskusteluja on avattu jo useamman muun maan jakelijan kanssa. Tavoitteena on saada luotua EU:n laajuinen jälleenmyyjäverkosto vuoden 2021 aikana. Tavoite on realistinen ja valitut ensimmäiset kumppanuudet isommissa Euroopan maissa osoittavat, että kandidaattien lista on toteuttamiskelpoinen ja vakuuttava. Yhteistyötä pohjoismaisten yliopistosairaaloiden kanssa jatketaan. Neuvottelut ovat olleet käynnissä johtavien pohjoismaisten yliopistosairaaloiden kanssa koko älyneulan historian ajan. Keskustelut ja aiemmat kliiniset kokeet useissa sairaaloissa ovat osoittaneet, että myynnin aloittamiselle on varsin hyvä pohja.
Kilpailutilanne
Lumbaalipunktioihin tarkoitettuja spinaalineuloja käytetään maailmassa paljon. Vuosittain tehdään noin 100 miljoonaa lumbaalipunktiota ja toimenpiteellä on yli sadan vuoden historia. Vallitseva käytäntö muodostaa sekä kilpailutekijän että mahdollisuuden. Mahdollisuus syntyy siitä, että nykykäytäntöön liittyy hankaluuksia ja riskejä, joita Injeq IQ-Tip®️ älyneulalla pystytään vähentämään. Kilpailutilanne puolestaan syntyy, kun hoitavien lääkärien mielestä vallitseva toimintatapa on riittävän toimiva ja edullinen. Kuitenkaan monet lastenlääkärit eivät ole tyytyväisiä nykyisiin ratkaisuihin, koska lumbaalipunktio etenkin lapsille on vaativa ja tavallisen neulan käyttöön liittyy tässä potilasryhmässä enemmän riskejä. Siksi yhtiö suuntaa voimavaransa ensin lasten tarpeisiin, minkä kautta odotetaan älyneulan käytön muodostuvan standardiksi myös aikuisten toimenpiteisiin.
Älykkäälle spinaalineulalle ei ole vielä omaa markkinasegmenttiä, koska tuotteita ei ole vielä kaupallisesti saatavilla. Injeq Oy on siten teknologia- ja toimialajohtaja tuotteen tullessa markkinoille. Vakiintuneet neulavalmistajat tuntevat yhtiön ja seuraavat sen edistymistä. Tähän on syytäkin, koska yhtiön visio on mullistaa vallitseva hoitokäytäntö. Tämä voi näkyä osalla neulavalmistajista heikentyneenä myyntinä. Sitä mukaa kun saavutamme tavoitteemme, perinteisten neulojen käyttö kyseisiin sovelluskohteisiin vähenee – sairaalaosasto kerrallaan. Toisaalta maailmanlaajuisilla markkinoilla on mahdollisuus olla partnerina perinteisten neulavalmistajien kanssa ja saada käyttöön heidän logistiikkansa sekä myynti- ja jakelukanavansa.
Lumbaalipunktioihin liittyvät ongelmat on laajalti tunnistettu ja kilpailevia ratkaisuja on pyritty kehittämään perustuen mm. neulan kärkeen kohdistuvan paineen tai heijastuvan valon mittaukseen. Kuitenkin esimerkiksi paineen mittaukseen, eli manometriin, perustuvaa tekniikka on käytöltään rajoittunutta, eikä valoon perustuvia ratkaisuja ole vielä kaupallistamisvaiheessa. Voidaan todeta, että vastaavaan toimintaan kykeneviä kilpailijoita ei markkinoilla ole ja heillä tuotteiden kehitystyö ja kaupallistaminen ovat Injeqiä jäljessä.
Laatujärjestelmä ja lääkinnällisen laitteen hyväksyminen
Lääkinnällisten terveydenhuollon laitteiden valmistus on viranomaisten säätelemää toimintaa. Viranomainen on ulkoistanut säädösten alaisen toiminnan valvonnan viranomaisten hyväksymille ilmoitetuille laitoksille. Säädösten perusteella Injeqillä tulee olla ilmoitetun laitoksen hyväksymä laatujärjestelmä, joka kattaa laitelainsäädännössä annetut minimivaatimukset. Vaatimukset ovat normaalia laatujärjestelmää vaativammat. Potilaalle aiheutuvan riskin minimoimiseksi hyväksyttävälle tasolle tulee esimerkiksi tuotteen kehitykseen, valmistukseen, tuotetestauksiin, potilastutkimuksiin, markkinointiin ja markkinoilla olevan tuotteen seurantaan liittyvien, laatujärjestelmässä kuvattujen toimenpiteiden olla hyväksytysti valmiina tuotaessa tuote markkinoille.
Tuotantomme siirtyi tuotantomittakaavaa vastaaviin uudet puhdastilat sisältäviin tiloihin kesällä 2019. Tarvittava, nyt sertifioitavana oleva laatujärjestelmä on ollut käytössä pidempään. Lopullinen tutkimuksiin perustuva kliininen näyttö arvioidaan saatavan hyväksytyksi ilmoitetun laitoksen toimesta yhtiön arvion mukaan alkuvuodesta 2021. Tämän rinnalla yhtiö on saamassa valmiiksi kaikki EU:n viranomaisvaatimusten mukaiset testaukset ja auditoinnit. Kun sertifiointi on saavutettu, yritys pyrkii hakemaan myyntilupia ensisijaisesti myös muilla maantieteellisillä alueilla, joissa hyväksytään CE-merkintä sellaisenaan tai kohtuullisin lisäyksin, sekä aloittamaan myöhemmin valmistelut muille suurimmille markkina-alueille (ml. USA, jossa vaaditaan oma FDA-hyväksyntäprosessi - The Food and Drug Administration).
Medical Device -asetus ja viranomaisvaatimukset
Uusien lääkinnällisten laitteiden kehitystyö ja kaupallistaminen regulatoristen vaatimusten mukaisesti ei aina ole suoraviivaista, mutta vastaavasti markkinoille pääsyn myötä asema on usein varsin kestävä. Keskeistä kaupallistamisessa on lääkinnällisiltä laitteilta vaadittavat viranomaishyväksynnät. Korkeasti säännellylle toimialalle säädettiin uusia vaatimuksia vuonna 2017. EU:n sääntelykehys muuttui direktiiveistä asetuksiin (MDD - Medical Device Directive; MDR - Medical Device Regulation) ja tulee suoraan sovellettaviksi kaikkien jäsenvaltioiden lainsäädäntöön. Lääkinnällisillä laitteilla direktiivin ja asetuksen välinen siirtymäaika päättyy toukokuussa 2021. Aiempaa vaativamman MD-asetuksen käytännöt eivät siten ole kaikilta osin vielä vakiintuneet. Muutoksen myötä myös sertifiointiprosessi on muuttunut vaativammaksi. Brexit ei myöskään helpottanut tilannetta, sillä lähes kolmasosa hyväksyntään tarvittavien ilmoitettujen laitosten resursseista oli Iso-Britanniassa. Kaikki tämä aiheuttaa tuotesertifiointien käsittelyssä huomattavaa ruuhkaa eurooppalaisten ilmoitettujen laitosten asiakkaille. MD-asetuksen mukaisten vaatimusten osalta Injeq on aloittanut ilmoitetun laitoksen TÜV SÜDin kanssa valmistelut jo vuonna 2018.

Kestävä kilpailuetu
Yhtiön tuotteet eivät ole helposti kilpailijoiden kopioitavissa. Sen paremmin neulan kuin tuotekokonaisuuteen kuuluvan analysaattorinkaan kopioiminen tai korvaaminen ei ole suoraviivaista ja niitä suojaamaan yhtiöllä on joko myönnettyjä tai haettuja patentteja neljästä eri teknologiasta. Patentit suojaavat yhtiön liiketoimintaa tietyiltä osin, ja kestävä kilpailuetu muodostuu patenttien ohella myös tutkimustyön ja kliinisten kokeiden tuottamasta tiedosta, jota ei voi patentoida eikä myöskään kopioida. Kilpailijoiden on myös käytävä lävitse vastaavat kliiniset kokeet, mikä antaa Injeqille selvän etumatkan markkinoilla.
Yhtiön tunnistusalgoritmit ovat salaisia ja mittaustietoa kertyy, kun tuotteita käytetään. Tämä mahdollistaa tuotteiden jatkuvan kehittämisen ja tunnistusalgoritmien optimoinnin. Yhtiön tavoite on, että Injeq IQ-Tip®️ älyneulan käyttö ajan myötä muodostuu parhaaksi hoitokäytännöksi.
Kasvupolut
Yhtiön ensimmäinen markkinasegmentti muodostuu eurooppalaisissa sairaaloissa tehtävistä lasten lumbaalipunktioista, erityisesti akuutin lymfaattisen leukemian (ALL) hoidossa tehtävistä pistoista. Onnistuminen tällä markkinalla on yhtiön keskeinen tavoite. Vuonna 2019 alkaneen 4-vuotisen monikansallisen ALLTogether-tutkimuksen tavoitteet ovat hyvin linjassa Injeqin älyneulan tuomien etujen kanssa. Jakelijoillemme Euroopassa tarjoutuu mahdollisuus liittyä ajankohtaisen eurooppalaisen tutkimuksen siivittämänä mukaan parantamaan ALL-lasten hoitoa ja ennustetta.
Ennakoivat toimenpiteet jakelija- ja myyntikanavien luomiseksi on aloitettu Euroopassa. Heti kun CE-merkki on myönnetty, on tavoitteemme laajentaa yhtiön toiminta maihin, jotka hyväksyvät sertifioinnin. Tämä antaa Injeqille huomattavan markkinapotentiaalin kaupallistamisen alkuvaiheessa. Kun ensisijainen sillanpääasema on varmistettu, kasvulle on olemassa useita muita reittejä. Panostukset näihin harkitaan tapauskohtaisesti. Keskeisiä tunnistettuja kasvupolkuja ovat mm. seuraavat:
- Aikuisten lumbaalipunktiot. Keskittyminen rajalliseen ja samalla tärkeään segmenttiin, kuten pediatrisiin hoitoihin, on järkevä tapa mennä markkinoille. Aikuisille tehdään kuitenkin lumbaalipunktioita ja selkäydinpuudutuksia huomattavasti enemmän kuin lapsille. Esimerkiksi selkäydinnesteen merkkiaineita käytetään enenevässä määrin tukemaan Alzheimerin taudin diagnostiikkaa (Paterson ym 2018). Ikääntyvä väestö ja Alzheimerin taudin esiintymisen yleistyminen kasvattavat diagnostisten lannepistojen määrää. Kun riittävä jalansija on saavutettu pediatrisessa käytössä ja teknologian hyödyt on osoitettu kliinikoille, on tarkoituksena käyttää pediatrisia osastoja referensseinä korostaen teknologian hyötyjä ja vähäisiä riskejä käytön laajentamiseksi lasten osastoilta myös aikuisten osastoille. Kunhan alkuvaiheen esteet on ylitetty ja IQ-Tip®️ menetelmä on markkinoilla hyväksytty, tämä siirtyminen on suhteellisen helppoa. Yhtiön näkökulmasta uusia laitteita tai jakelijoita ei tällöin tarvita eikä kliinikkojen tarvitse oppia uusia taitoja. Yhtiö odottaa, että ajan mittaan älyneula on osa normaalia diagnostiikkaa ja hoitokäytäntöjä, koska digitaaliteknologian tarjoamaa helppoutta ja turvallisuutta arvostetaan suuresti. Älyneulaa voidaan lisäksi käyttää uusien terveydenhuollon ammattilaisten koulutuksessa. Tämä asiakastarve on tullut selkeästi esiin tutkimusten yhteydessä.
- Myynnin laajentaminen muualle maailmaan. Panostaminen lasten hyvinvointiin on kasvualue myös Euroopan ja Yhdysvaltojen ulkopuolella. Eurooppalainen tuotehyväksyntä toimii hyvänä pohjana useiden maiden hyväksyntäprosesseille. Uusien myyntilupien ja myyntiverkoston laajentamista harkitaan EU-hyväksynnän jälkeen.
- Valmistelut FDA-hyväksynnän hakemiseksi ja myynnin laajentaminen Pohjois-Amerikkaan. Valmistelut seuraavan, FDA-hyväksyntäprosessin käynnistämiseksi uusien potilastutkimusten ohella voidaan aloittaa sen jälkeen, kun EU-hyväksyntä (CE-merkki) on myönnetty IQ-Tip®️ -tuotteelle ja tuote on markkinoilla. Yhdysvallat tarjoaa merkittäviä mahdollisuuksia maailman suurimpana terveydenhuollon tuotteiden markkinana.
- Uudet tuotealueet. Lumbaalipunktion lisäksi IQ-Tip®️ -teknologiaa voidaan käyttää myös monissa muissa vaativissa toimenpiteissä, kuten nivel- ja verisuonipistoissa, näytepalojen otossa, eläinlääketieteessä, ensihoidossa jne. Yhtiö selvittää vaihtoehtoisia mahdollisuuksia näillä sovellusalueilla sen jälkeen, kun älyneulan ensimmäinen sovellus on tuotu markkinoille.
Tiimimme
Terveysteknologian kaupallinen merkitys Suomessa on kasvanut vuosi vuodelta. Nykyään alan vienti on yksi nopeimmin kasvavista korkean teknologian aloista Suomessa (Healthtech Finland export statistics). Injeq toimii Tampereella, missä yhteistyö Tampereen yliopiston ja yliopistosairaalan kanssa on viime vuosikymmenien aikana rakentanut toimivan ekosysteemin tutkimuksen ja yritysten välille. Tampereella asiantuntijoita löytyy, mutta toisaalta parhaista resursseista käydään kilpailua.
Näistä lähtökohdista Injeq on saanut koottua osaavan ja kokeneen tiimiin. Tiimi koostuu ammattilaisista, joilla on kokemusta laajalta alueelta kattaen mm. lääketieteellisen ja kliinisen tutkimuksen, viranomaisvaatimukset ja signaalinkäsittelyn sekä myynnin, tuotannon, laadunvarmistuksen ja kansainvälisen johtamisen osa-alueet. Yrityksellä on aktiivinen hallitus, jossa toimii innovaation alkuperäisiä kehittäjiä ja asiantuntijoita. Hallitusta tukevat myös ulkoiset neuvonantajat, jotka haluavat siivittää IQ-Tip® tuotteet menestykseen.

Tuotantotalouden DI, 30 vuoden kokemus kansainvälisistä myynti-, markkinointi- ja johtotehtävistä useissa Euroopan maissa globaalien terveysteknologian markkinajohtajien organisaatioissa ja pk-/startup-yritysten johdossa. Yhdessä asiantuntijatiimien kanssa kaupallistanut kymmeniä järjestelmiä ja satoja tuotteita globaaleille terveydenhoitoalan markkinoille.

Kokenut kansainvälisen myynnin ammattilainen yli 30 vuoden kokemuksella teknologian myynnistä. Vastaa myyntikanavan ja jakelijakumppanuuksien kehittämisestä.

Kliininen asiantuntija, tuotespesialisti, myynnin tuki ja jakelijoiden koulutukset. Biolääketieteen laitokselta valmistunut diplomi-insinööri, anestesiaerikoissairaanhoitaja, sertifioitu ISO 13485: 2016 Lead Auditor 2020. Vuosien kokemus kansainvälisestä jakelijayhteistyöstä Euroopan markkinoilla, myynti- ja koulutustilaisuuksien organisoinnista ja eurooppalaisesta tutkimuksesta.

Tuotantotalouden DI yli 20 vuoden kokemuksella innovatiivisten high-tech tuotteiden parissa. Vastaa tuotekehityksestä sekä monista yleisjohdon tehtävistä.

Tekniikan tohtori ja lääketieteellisen tekniikan dosentti. Yli 30 vuoden kokemus kliinisten ja kokeellisten tutkimusten tekemisestä ja soveltamisesta lääkinnällisiin laitteisiin. Yli 320 vertaisarvioitua kansainvälistä tieteellistä julkaisua. Vastaa kliinisestä tutkimustoiminnasta.

Lääketieteellisen fysiikan DI. Kliinisten tutkimusten ja kliinisen arvioinnin, tuotteiden verifiointi- ja validointitestauksen sekä datan analysoinnin asiantuntija.

Biomittausten DI, Tohtorikoulutettava. Kliinisten tutkimusten ja datan analysoinnin asiantuntija.

MMM, pääaine mikrobiologia. Yli 20 vuoden kokemus laatutyöstä mikrobiologian ja laadunvalvonnan alueilla lääkkeiden ja lääketieteellisen teknologian tuotteiden kehityksessä ja valmistuksessa.

Valmistusteknologian DI yli 20 vuoden kokemuksella. Vastaa tuotannosta sekä tuotantoprosessien, -menetelmien, -tilojen ja -laitteiden kehittämisestä.

Tuotannon ylläpito, monitorointi ja testaus. Puhdastilaspesialisti.

Tuotteiden valmistus, tuotantoprosessin kehitys sekä perehdytys.
Tuotteiden valmistus. 20 vuoden kokemus lääketieteellisten laitteiden valmistuksesta.

Tuotteiden valmistus, tuotantoprosessin kehitys sekä perehdytys.

Hallitusammattilainen yli 30 vuoden yrittäjäkokemuksella. Väitellyt tekniikan tohtoriksi kasvuyritystoiminnasta. Hallituksen puheenjohtajana vastannut strategisesta suunnittelusta, liiketoiminnan kehittämisestä ja rahoituksesta.

Professori, lääketieteen tohtori, hammaslääketieteen lisensiaatti, suu- ja leukakirurgian erikoislääkäri ja erikoishammaslääkäri. Yli 30 vuotta kokemusta kliinisestä työstä, tutkimuksesta ja yritystoiminnasta.

Tekniikan tohtori ja lääketieteellisen tekniikan professori. 30 vuoden kokemus lääkintälaitteiden ja lääketieteellisen tekniikan tutkimuksesta ja opetuksesta sekä yli 15 vuoden kokemus tutkimustoiminnan ja kansainvälisten järjestöjen johtotehtävistä.

Hammaslääketieteen lisensiaatti ja diplomi-insinööri. Alkuperäisen älyneulan kehittäjä.

DI. Toimitusjohtaja lääkinnällisiä laitteita valmistavassa Atrotech Oy:ssä.

BBA & MBA, HHJ. Terveysteknologian ja johtamisen ammattilainen.

Lääketieteen ja kirurgian tohtori. Teoreettinen ja käytännön tuntemus kliinisestä työstä yhdistettynä alan verkostoihin.

Anestesian professori emerita. Kattava käytännön ja teoreettinen tuntemus ja osaaminen mm. neulojen ja sokeiden pistojen alueilla.

Tekniikan lisensiaatti. Toimii kehitysjohtajana TAYS TKI-keskuksessa. Viranomaissäätelyn erikoisasiantuntija ja kirjan: "The Survival Guide to EU Medical Device Regulations" kirjoittaja.

Kauppatieteiden maisteri. Kokenut pääomasijoittamisen ammattilainen sekä analyytikko. Edustaa EAKR Aloitusrahastoa.
Rahojen käyttötarkoitus
Arvonmääritys
Kirjaudu sisään
Sisältö on saatavilla vain sijoittajille jotka ovat sijoittaneet tähän rahoituskierrokseen.
Tietoa annin ehdoista
Kirjaudu sisään
Sisältö on saatavilla vain sijoittajille jotka ovat sijoittaneet tähän rahoituskierrokseen.
Taloustiedot
Kirjaudu sisään
Sisältö on saatavilla vain sijoittajille jotka ovat sijoittaneet tähän rahoituskierrokseen.
Riskit
Kirjaudu sisään
Sisältö on saatavilla vain sijoittajille jotka ovat sijoittaneet tähän rahoituskierrokseen.
Liitteet
Kirjaudu sisään
Sisältö on saatavilla vain sijoittajille jotka ovat sijoittaneet tähän rahoituskierrokseen.
Päivityksiä
Kirjaudu sisään
Sisältö on saatavilla vain sijoittajille jotka ovat sijoittaneet tähän rahoituskierrokseen.
